ΚΑΙ ΣΤΟ ΤΕΛΟΣ ΔΕΝ ΕΜΕΙΝΕ ΚΑΝΕΙΣ: Η ΑΠΟΛΥΤΗ ΚΑΤΑΣΤΡΟΦΗ ΤΗΣ ΜΙΚΡΟΑΓΓΕΙΩΣΗΣ ΑΠΟ ΤΗ ΠΡΩΤΕΪΝΗ ΑΚΙΔΑ ΚΑΙ Η ΠΑΘΟΦΥΣΙΟΛΟΓΙΑ ΤΟΥ COVID, του Μακροχρόνιου COVID και του Συνδρόμου Αιφνίδιου Θανάτου
Η ΠΡΩΤΕΪΝΗ ΑΚΙΔΑΣ ΕΧΕΙ ΕΝΑ «ΜΟΝΑΔΙΚΟ» ΜΗΧΑΝΙΣΜΟ ΓΙΑ ΝΑ ΠΡΟΚΑΛΕΙ ΖΗΜΙΑ ΕΝΩ ΤΑΥΤΟΧΡΟΝΑ ΕΜΠΟΔΙΖΕΙ ΤΗΝ ΑΠΑΝΤΗΣΗ ΠΟΥ ΧΡΕΙΑΖΕΤΑΙ ΓΙΑ ΤΗΝ ΕΠΙΣΚΕΥΗ ΑΥΤΗΣ ΤΗΣ ΖΗΜΙΑΣ! ΑΝ ΔΕΝ ΕΙΝΑΙ ΒΙΟΛΟΓΙΚΟ ΟΠΛΟ ΤΟΤΕ ΤΙ ΕΙΝΑΙ;
Εάν η αρχική επίθεσή στο ενδοθήλιο δεν είναι θανατηφόρα, τότε θα είναι οι επαναλαμβανόμενοι κύκλοι επούλωσης αυτού
Του Walter M Chesnut
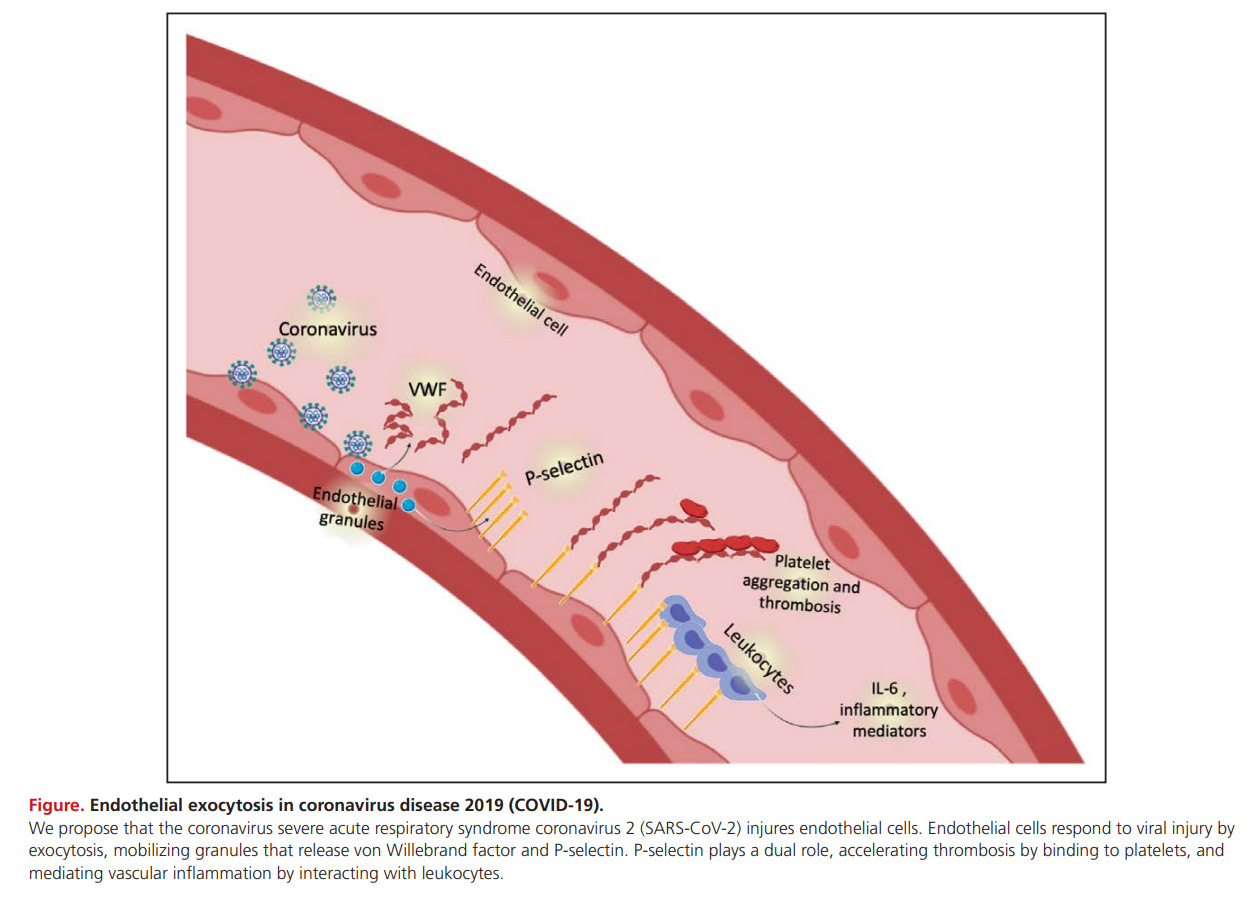
Είναι καλά κατανοητό ότι ο πρωταρχικός μηχανισμός του θανάτου στη νόσο COVID-19 είναι μικροαγγειακής φύσης.
Η σοβαρή νόσος COVID-19 είναι μια μικροαγγειακή νόσος
https://www.ahajournals.org/doi/pdf/10.1161/CIRCULATIONAHA.120.050354
Είναι επίσης καλά κατανοητό ότι η πρωτεΐνη Ακίδας βλάπτει το Ενδοθήλιο και τα Ενδοθηλιακά Μιτοχόνδρια.
Αν και η χρήση ενός μη μολυσματικού ψευδοϊού αποτελεί περιορισμό σε αυτή τη μελέτη, τα δεδομένα μας αποκαλύπτουν ότι η πρωτεΐνη Ακίδας S από μόνη της μπορεί να βλάψει το ενδοθήλιο, που εκδηλώνεται με μειωμένη μιτοχονδριακή λειτουργία και δραστηριότητα του γονιδίου της ενδοθηλιακής συνθετάσης του μονοξειδίου του αζώτου (eNOS) εκτός από αυξημένη γλυκόλυση. Φαίνεται ότι η πρωτεΐνη S στα ενδοθηλιακά κύτταρα (ECs) αυξάνει το οξειδοαναγωγικό/οξειδωτικό στρες (redox stress) που μπορεί να οδηγήσει σε απενεργοποίηση της AMPK1 (πρωτεϊνική κινάση που ενεργοποιείται από τη μονοφωσφορική αδενοσίνη), ανοδική ρύθμιση της πρωτεινης MDM22 (σ.σ. που δημιουργεί καρκινογενεσεις) και τελικά αποσταθεροποίηση του υποδοχέα ACE2.
Η πρωτεΐνη Ακίδας του SARS-CoV-2 επηρεάζει την ενδοθηλιακή λειτουργία μέσω της καταστολής του υποδοχέα ACE 2
https://www.ahajournals.org/doi/full/10.1161/CIRCRESAHA.121.318902
Ωστόσο, αυτό που πιστεύω δεν έχει γίνει ακόμη καλά κατανοητό είναι ότι εάν ο θύμα επιζεί από τη λοίμωξη του SARS-CoV-2, ή από την έκθεση στην πρωτεΐνη Ακίδας, ωστόσο έχει γίνει μη αναστρέψιμη η βλάβη στο μικροαγγειακό σύστημα του σώματος. Είναι ενδιαφέρον ότι ο μηχανισμός αυτής της βλάβης είναι ΑΚΡΙΒΩΣ Ο ΙΔΙΟΣ με τον μηχανισμό της ενδοθηλιακής βλάβης στον ΔΙΑΒΗΤΗ: Η ΠΑΘΟΛΟΓΙΚΗ ΑΝΙΣΟΡΡΟΠΙΑ ΤΗΣ ΕΝΔΟΘΗΛΙΑΚΗΣ ΒΛΑΒΗΣ ΚΑΙ ΕΠΙΔΙΟΡΘΩΣΗΣ.
Στην υγεία, η αθροιστική βλάβη στα ενδοθηλιακά κύτταρα που προκαλείται από την έκθεση σε παράγοντες κινδύνου μετριάζεται από ενδογενείς επανορθωτικές διεργασίες. Η διαταραχή της ισορροπίας μεταξύ της ενδοθηλιακής βλάβης και της αποκατάστασης μπορεί να μεσολαβήσει στην αθηροσκληρωτική εξέλιξη. Τα «ενδοθηλιακά προγονικά κύτταρα» (EPC) που προέρχονται από τον μυελό των οστών έχουν αναγνωριστεί ως σημαντικοί παράγοντες που συμβάλλουν στην ενδογενή αγγειακή αποκατάσταση. Η αντίσταση στην ινσουλίνη σχετίζεται με ένα φάσμα βιοχημικών ανωμαλιών που έχουν τη δυναμική να μειώσουν τη διαθεσιμότητα των EPC και να μειώσουν την ικανότητά τους για αγγειακή επιδιόρθωση.
Η επίδραση της αντίστασης στην ινσουλίνη στη λειτουργία του ενδοθηλίου, στα προγονικά κύτταρα και στην επιδιόρθωση
https://journals.sagepub.com/doi/pdf/10.3132/dvdr.2007.027
Η ΜΟΝΗ ΕΞΑΙΡΕΣΗ! Όσον αφορά τη COVID-19 και την πρωτεΐνη Ακίδας, δεν είναι η ΙΝΣΟΥΛΙΝΗ που επηρεάζει τη διαθεσιμότητα των Ενδοθηλιακών Προγονικών Κυττάρων (EPC). Είναι η ΠΡΩΤΕΪΝΗ ΑΚΙΔΑΣ!
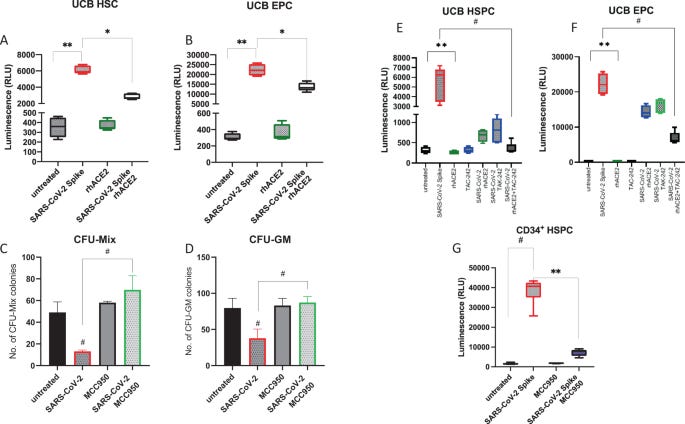
Αυξανόμενα στοιχεία συσσωρεύονται που δειχνουν ότι τα αιμοποιητικά βλαστοκύτταρα/προγονικά κύτταρα (HSPC) και τα ενδοθηλιακά προγονικά κύτταρα (EPC) έχουν υποστεί βλάβη κατά τη διάρκεια σοβαρής λοίμωξης SARS-Cov-2/COVID-19. Έχει αναφερθεί ότι ασθενείς που έχουν μολυνθεί με COVID-19 εμφανίζονται συχνά με αναιμία, λεμφοπενία και θρομβοπενία. Αυτή η αρνητική επίδραση του ιού στην ανθρώπινη αιμοποίηση και το ενδοθήλιο έχει αναφερθεί σε μολυσμένους ασθενείς και έχει αποδειχθεί in vitro μετά από έκθεση των κυττάρων στην πρωτεΐνη ακίδας του SARS-Cov-2/COVID-19 (SP).
Μια απόδειξη ότι η πρωτεΐνη ακίδας του SARS-Cov-2/COVID-19 καταστρέφει τα αιμοποιητικά βλαστοκύτταρα/προγονικά κύτταρα στον μηχανισμό της Πυρόπτωσης3 με τρόπο εξαρτώμενο από το φλεγμονόσωμα NLRP34
https://www.nature.com/articles/s41375-021- 01332-z
Και εδώ, πιστεύω, είναι το κύριο πρόβλημα:
Τόσο τα Ενδοθηλιακά Κύτταρα (ECs) όσο και τα Αγγειακά Λεία Μυϊκά Κύτταρα (SMCs) χρειάζονται για την αναγέννηση των περιφερικών αρτηριών στους ισχαιμικούς ιστούς.
Συγχορήγηση Ενδοθηλιακών και Λείων Μυϊκών Κυττάρων που προέρχονται από ανθρώπινα πολυδύναμα βλαστοκύτταρα ως θεραπεία για την κρίσιμη ισχαιμία των άκρων
https://stemcellsjournals.onlinelibrary.wiley.com/doi/full/10.1002/sctm.20-0132
Ωστόσο, δεν υπάρχουν αρκετά Ενδοθηλιακά Προγονικά Κύτταρα (EPCs) διαθέσιμα για την αποκατάσταση της βλάβης. Είναι σαν να προσπαθείς να φτιάξεις μια σάλτσα Ολαντέζ μόνο με κρόκους αυγών – αλλά χωρίς βούτυρο. Πιστεύω ότι αυτό εξηγεί τη στένωση του αυλού (σ.σ. κοιλότητα/κανάλι του αγγείου μέσα στην οποία ρέει το αίμα) που πιστεύω ότι συμβαίνει λόγω αυτής της μειωμένης διαδικασίας επισκευής. Αποδίδοντας τα ίδια αποτελέσματα με τη μειωμένη απόκριση επιδιόρθωσης των μικροαγγείων που παρατηρείται και στον Διαβήτη.
Οι διαβητικοί ασθενείς έχουν αυξημένο πολλαπλασιασμό των Λείων Μυικών Αγγειακών Κυττάρων (VSMC) και ενεργοποιούν έναν πιο συνθετικό φαινότυπο συμβατό με αγγειακή δυσλειτουργία, η οποία μπορεί να προκαλέσει πάχυνση της έσω στιβάδας και στένωση του αυλού της αρτηρίας που οδηγεί σε ισχαιμία.
Διαβητική αγγειοπάθεια: μακρο- και μικροαγγειακή βλάβη
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7351096/
Έτσι, όπως μπορεί κανείς να συμπεράνει, εάν ένα κατεστραμμένο ενδοθήλιο ΑΝΑΚΑΤΑΣΚΕΥΑΖΕΤΑΙ και ΑΝΑΚΑΤΑΣΚΕΥΑΖΕΤΑΙ ξανά και ξανά, και ΔΕΝ ΜΠΟΡΕΙ ΝΑ ΕΠΟΥΛΩΘΕΙ ΣΩΣΤΑ ΚΑΘΕ ΦΟΡΑ, τελικά το μικροαγγειακό σύστημα θα καταστραφεί - και θα γίνει ουλώδης ιστός και/ή λείος μυς.
Δυστυχώς, δεν πιστεύω ότι αυτός είναι ο μόνος θανατηφόρος μηχανισμός της πρωτεΐνης Ακίδας. Από ότι έχω παρατηρήσει, η πρωτεΐνη Ακίδας έχει το «μοναδικό» (τουλάχιστον) μηχανισμό για να ΠΡΟΚΑΛΕΙ ΖΗΜΙΑ ΚΑΙ ΤΑΥΤΟΧΡΟΝΑ ΝΑ ΕΜΠΟΔΙΖΕΙ ΤΗΝ ΑΠΑΝΤΗΣΗ ΠΟΥ ΧΡΕΙΑΖΕΤΑΙ ΓΙΑ ΤΗΝ ΕΠΙΣΚΕΥΗ ΑΥΤΗΣ ΤΗΣ ΖΗΜΙΑΣ.
Αυτή ήταν μια πλήρης εξήγηση του πώς η πρωτεΐνη Ακίδας προκαλεί είτε άμεσα είτε σταδιακά θανατηφόρα μικροαγγειακή βλάβη. Εργάζομαι πάνω στη λεπτομέρεια πώς αυτό επηρεάζει όλα τα συστήματα του σώματος και πώς αυτό εξηγεί τα παρατηρούμενα συμπτώματα του μακροχρόνιου COVID και τη δραματική αύξηση του Συνδρόμου Αιφνίδιου Θανάτου λόγω Αρρυθμίας (SADS).
Η AMPK (πρωτεϊνική κινάση που ενεργοποιείται από τη μονοφωσφορική αδενοσίνη) είναι ένα ένζυμο που δρα ως μεταβολικός διακόπτης. Έχει περιγραφεί ως «μαγική» πρωτεΐνη, προσφέροντας ευρεία ευεργετικά αποτελέσματα στην υγεία, από τη βελτίωση της καρδιαγγειακής υγείας έως την παράταση της διάρκειας ζωής. Ενεργοποιείται ως απόκριση σε χαμηλά επίπεδα κυτταρικής ενέργειας, όπως παρατηρείται συχνά κατά τη διάρκεια της άσκησης ή περιόδους περιορισμού των θερμίδων. Σχετικές έρευνες διαπίστωσαν ότι η ενεργοποίηση της AMPK οδηγεί σε αξιοσημείωτες αυξήσεις στη διάρκεια ζωής ενώ η απενεργοποίηση της οδηγεί σε γήρανση και πρόκλησή αιφνίδιου θανάτου.
Η MDM2 είναι μια κυτταρική φωσφοπρωτεΐνη που σχηματίζει ένα σύμπλεγμα με την ογκοκατασταλτική πρωτεΐνη p53 (σ.σ. τον Φύλακα του Γονιδιώματος). Η MDM2 έχει μία δραστηριότητα την Ε3 λιγάση ουβικιτίνης, η οποία παίζει κρίσιμο ρόλο στην υποβάθμιση της p53. Η MDM2 υπερεκφράζεται σε πολλές ανθρώπινες κακοήθειες, υποδεικνύοντας ότι είναι ένας σημαντικός μηχανισμός που χρησιμοποιείται από τα καρκινικά κύτταρα για να ξεφύγουν από την επιτήρηση της p53.
Η Πυρόπτωση είναι μια άκρως φλεγμονώδης μορφή λυτικού προγραμματισμένου κυτταρικού θανάτου, που εμφανίζεται συχνότερα κατά τη μόλυνση με ενδοκυτταρικά παθογόνα και είναι πιθανό να αποτελεί μέρος της αντιμικροβιακής απόκρισης.
Η υπερενεργοποίηση του φλεγμονοσώματος NLRP3 έχει συνδεθεί με μια ποικιλία χρόνιων παθήσεων, συμπεριλαμβανομένης της σκλήρυνσης κατά πλάκας, του καρκίνου, του διαβήτη και της άνοιας.